Здесь легко и интересно общаться. Присоединяйся!
ты что рехнулся задавать такие вопросы простым людям или в школе не доучили
CxHy+(x+y/2)/2O2=xCO2+y/2H2O
n(C)=m cмеси * w(C) / M(C) = 240*0.86/12=17.2 моль
n(H)= m cмеси * w(H) / M(H) = 240*0.14/1= 33.6 моль
n(O) в CO2 = n(C)*2
n(O) в H2O = n(H)/2
Значит n(O)=2*n(C)+n(H)/2=17.2*2+33.6/2=51.2 моль
Тогда n(O2)=n(O)/2 = 51.2/2= 25.6 моль
Пересчитаем количество кислорода на воздух
n(воздух)=n(O2)*100%/21%=25.6*100/21=121.9 моль
V(воздух)=n(воздух)*Vm=121,9*22,4=2730,7 дм³ ≈2,73 м³
(0) СПАСИБО (2)
Определить объем воздуха, необходимого для горения 5м 3 смеси газов, состоящих из 20% СН4, 10% СО, 5%N, 35%О2, если коэффициент избытка воздуха равен 1,8.
Решение:Горючее-смесь газов. Поэтому для расчета объема воздуха, пошедшего на сгорание, воспользуемся формулой (1.5). Для определения стехиометрических коэффициентов при кислороде nо2 запишем уравнение реакции горения горючих компонентов в кислороде:
V 0 B= 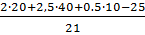
Для горения 5м 3 газовой смеси необходимый теоретический объем воздуха составит: V 0 B=5∙5,7 =32,5 м 3 Практическое количество воздуха : V 0 B=1,8∙32,5=58,5 м 3 .
Пример №5.
Определите коэффициент избытка воздуха при горении уксусной кислоты, если на горение 1кг поступило 3 м 3 воздуха.
Решение: Для определения коэффициента избытка воздуха по формуле (1.7) необходимо рассчитать его теоретическое количество. Молекулярная масса уксусной кислоты-60.
V 0 B= 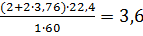
тогда коэффициент избытка воздуха равен:
Горение протекало при недостатке воздуха.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Сдача сессии и защита диплома — страшная бессонница, которая потом кажется страшным сном. 8913 — 

91.146.8.87 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
Ответ или решение 1
Реакция окисления этана описывается следующим уравнением химической реакции.
В соответствии с коэффициентами этого уравнения для окисления 1 молекула пропана требуется 5 молекул кислорода. При этом синтезируется 3 молекулы углекислого газа.
Вычислим имеющееся количество пропана.
Для этого поделим имеющийся объем газа на объем 1 моля идеального газа при нормальных условиях.
N С3Н8 = 100 / 22,4 = 4,46 моль; Количество кислорода составит.
N O2 = 4,46 х 5 = 22,3 моль;
Вычислим объем газа. Для этого умножим количество вещества на объем 1 моля газа.
Его объем составит: V O2 = 22,3 х 22,4 = 500 литров;
С учетом содержания кислорода в воздухе 21% необходимый объем воздуха составит: